Larutan Elektrolit & Nonelektrolit: Pengerian, Ciri, Jenis dan Contohnya Lengkap
https://blogmipa-kimia.blogspot.com/2018/01/larutan-elekrolit-dan-elektrolit.html
Daftar Materi Kimia
Advertisement
Baca Juga:
Pengertian Larutan Elektrolit dan Nonelektrolit
Pernahkah kalian melihat seseorang mencari ikan dengan cara menyetrum? Apa yang terjadi setelah beberapa saat ujung alat yang telah dialiri listrik itu dicelupkan ke dalam air sungai? Ternyata, ikan-ikan yang berada di sekitar alat itu terkena aliran listrik, kemudian pingsan atau mati. Apakah air dapat menghantarkan listrik?
Air murni adalah penghantar listrik yang buruk, tetapi jika dilarutkan garam dapur, maka larutan ini dapat menghantarkan arus listrik. Sebaliknya, jika ke dalam air dilarutkan gula tebu, ternyata daya hantar listrik larutan tidak berbeda dengan air murni. Dengan kata lain larutan gula tebu merupakan penghantar listrik yang buruk.
Bagaimana cara mengetahui apakah suatu larutan merupakan larutan elektrolit atau nonelektrolit? Untuk mengetahuinya, kalian dapat melakukan praktikum atau percobaan berikut ini untuk menumbuhkan etos kerja, mengembangkan kecakapan sosial dan vokasional kalian.
Ekperimen: Daya Hantar Listrik Larutan
Tujuan:
Menguji daya hantar listrik beberapa larutan serta mengamati gejala berlangsungnya hantaran arus listrik.
Alat:
■ Seperangkat alat uji elektrolit dengan sumber baterai (9 V) dan elektroda grafit
■ Gelas kimia.
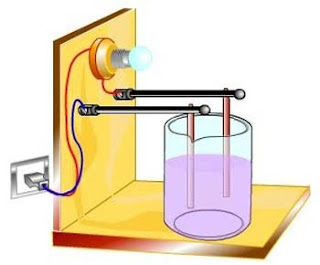
Ilustrasi alat uji daya hantar listrik larutan diperlihatkan pada gambar berikut ini.
Bahan:
■ Larutan CH3COOH 1 M
■ Larutan NH4OH 1 M
■ Larutan NaOH 1 M
■ Larutan HCl 1 M
■ Akuades (air suling)
■ Larutan NaCl 1 M
■ Larutan gula 10%
■ Larutan urea 10%
■ Larutan alkohol 10%
Cara Kerja:
1. Masukkan akuades (air suling) ke dalam gelas kimia hingga terisi ¾-nya. Ujilah daya hantar akuades ini dengan menyambungkan alat dengan sumber arus. Jika lampu pada alat uji tidak menyala, maka alat dapat digunakan untuk menguji larutan lainnya. Jika lampu menyala (walaupun redup), maka alat perlu dibersihkan lagi (terutama elektroda dan gelas kimia).
2. Masukkan tiap-tiap larutan ke dalam gelas alat uji hingga terisi ¾-nya. Jika memungkinkan, sebaiknya percobaan untuk beberapa larutan dilakukan secara bersamaan sehingga dapat diamati dan di bandingkan gejala hantaran arus listrik yang terjadi.
3. Jika tidak memungkinkan, maka setiap kali setelah menguji daya hantar listrik suatu larutan, gelas dan elektroda pada alat uji harus dibersihkan terlebih dahulu dengan akuades lalu dilap hingga kering sebelum digunakan untuk menguji larutan berikutnya.
4. Amati perubahan wujud yang terjadi, intensitas nyala lampu (terang, redup atau tidak menyala) dan gejala yang terjadi di sekitar elektroda yang tercelup dalam larutan (ada gelembung gas atau tidak).
5. Mencatat perubahan yang terjadi tersebut dalam tabel pengamatan.
Tabel Pengamatan:
No.
|
Larutan Uji
|
Bola Lampu
(Menyala/Tidak)
|
Gelembung Gas
(Ada/Tidak)
|
Keterangan
|
1.
|
Gula
|
………………………
|
………………………
|
………………………
|
2.
|
Urea
|
………………………
|
………………………
|
………………………
|
3.
|
Alohol
|
………………………
|
………………………
|
………………………
|
4.
|
CH3COOOH
|
………………………
|
………………………
|
………………………
|
5.
|
NH4OH
|
………………………
|
………………………
|
………………………
|
6.
|
HCl
|
………………………
|
………………………
|
………………………
|
7.
|
NaOH
|
………………………
|
………………………
|
………………………
|
8.
|
NaCl
|
………………………
|
………………………
|
………………………
|
Pertanyaan:
1. Berdasarkan hasil percobaan, sebutkan gejala-gejala apa saja yang menandai berlangsungnya hantaran arus listrik pada larutan!
2. Kelompokkan larutan uji tersebut ke dalam kelompok larutan yang dapat menghantarkan arus listrik (larutan elektrolit) dan larutan yang tidak dapat menghantarkan arus listrik (larutan nonelektrolit).
Berdasarkan daya hantar listriknya, larutan dapat dibedakan menjadi dua, yakni larutan elektrolit dan larutan nonelektrolit.
■ Larutan elektrolit adalah larutan yang dapat menghantarkan arus listrik.
■ Larutan nonelektrolit adalah larutan yang tidak dapat menghantarkan arus listrik.
Tanah maupun air limbah mengandung berbagai jenis elektrolit sehingga genangan air, air sungai, atau air selokan dapat menghantarkan listrik.
Ciri-Ciri Larutan Elektrolit dan Nonelektrolit
Berdasarkan hasil eksperimen sebelumnya, kalian tentu sudah dapat menentukan jenis larutan berdasarkan daya hantar listriknya, larutan mana yang bersifat elektrolit dan larutan mana yang bersifat non elektrolit. Kalian juga pasti sudah dapat menentukan gejala apa yang akan terjadi pada alat uji ketika suatu larutan dialiri arus listrik, baik gejala untuk larutan elektrolit maupun larutan non-elektrolit.
Larutan yang dapat menghantarkan arus listrik memberikan gejala berupa menyalanya lampu pada alat uji dan atau timbulnya gelembung gas pada elektroda yang tercelup dalam larutan, sehinga larutan yang menunjukkan gejala-gejala tersebut pada pengujian daya hantar tergolong sebagai larutan elektrolit.
Sebaliknya larutan yang tidak menunjukkan adanya gejala-gejala tersebut, berarti larutan tersebut tidak dapat menghantarkan arus listrik dan digolongkan sebagai larutan nonelektrolit. Sekarang coba kalian perhatikan hasil pengujian daya hantar listrik pada tabel berikut ini.
Tabel Hasil Pengujian Daya hantar Listrik
Larutan
|
Nyala Lampu
|
Gelembung gas
| |||
Terang
|
Redup
|
Tidak menyala
|
Ada
|
Tidak ada
| |
Larutan urea
|
−
|
−
|
√
|
−
|
√
|
Larutan amonia
|
−
|
√
|
−
|
√
|
−
|
Larutan HCl
|
√
|
−
|
−
|
√
|
−
|
Larutan cuka
|
−
|
√
|
−
|
√
|
−
|
Larutan H2SO4
|
√
|
−
|
−
|
√
|
−
|
Larutan alkohol
|
−
|
−
|
√
|
−
|
√
|
Air laut
|
√
|
−
|
−
|
√
|
−
|
Larutan H2S
|
−
|
√
|
−
|
√
|
−
|
Air kapur
|
√
|
−
|
−
|
√
|
−
|
Larutan glukosa
|
−
|
−
|
√
|
−
|
√
|
Dari hasil pengujian pada tabel hasil pengujian daya hantar listrik tersebut, dapat disimpulkan bahwa larutan yang dapat menghantarkan arus listrik, yaitu larutan amonia, larutan HCl, larutan cuka, larutan H2SO4, air laut, air kapur, dan larutan H2S. Sedangkan larutan yang tidak dapat menghantarkan arus listrik, di antaranya adalah larutan urea, larutan alkohol, dan larutan glukosa.
Jenis Larutan Elektrolit dan Nonelektrolit
Perhatikan kembali data larutan yang bersifat elektrolit. Daya hantar larutan elektrolit bergantung pada jenis dan konsentrasinya. Larutan yang mempunyai daya hantar relatif baik walaupun konsentrasinya relatif rendah disebut larutan elektrolit kuat. Contoh larutan elektrolit kuat ini antara lain larutan HCl, H2SO4, air laut, dan air kapur.
Sebaliknya, larutan yang daya hantarnya buruk walaupun konsentrasinya relatif besar disebut larutan elektrolit lemah. Contoh larutan elektrolit lemah antara lain larutan amonia, larutan cuka, dan larutan H2S.
Pada konsentrasi yang sama, larutan elektrolit kuat menghantarkan listrik lebih baik daripada larutan elektrolit lemah. Baik tidaknya daya hantar listrik suatu larutan dapat diketahui dari intensitas nyala lampu dan ada tidaknya gelembung gas.
Ternyata ada larutan elektrolit yang memberikan gejala berupa menyalanya lampu pada alat uji dan ada pula yang tidak. Namun, semuanya menimbulkan gejala berupa adanya gelembung gas pada elektroda yang tercelup dalam larutan. Perhatikan gambar berikut ini. Apakah perbedaan dari ketiga gambar tersebut.
Larutan elektrolit kuat terbentuk dari senyawa elektrolit kuat yang terlarut dalam pelarut air. Senyawa elektrolit kuat dalam air terurai sempurna (atau hampir sempurna) membentuk ion positif (kation) dan ion negatif (anion). Misalnya senyawa elektrolit NaCl dalam pelarut air terurai menjadi ion-ionnya, yaitu Na+ dan Cl-.
Sebagaimana kita ketahui bahwa arus listrik merupakan jumlah elektron per detik. Pada saat elektron-elektron dilewatkan ke dalam larutan elektrolit kuat, elektron tersebut dapat dihantarkan (dibawa) oleh ion-ion yang mampu bergerak bebas dalam larutannya tersebut seperti dihantarkan oleh kabel tembaga. Aliran arus listrik kemudian dapat diamati dan diketahui dari gejala berupa menyalanya lampu pada alat uji.
Pada larutan elektrolit lemah, walaupun terbentuk ion, tetapi ion-ion (kation dan anion) yang terbentuk jumlahnya sangat sedikit. Akibatnya, ion-ion tersebut tidak dapat menghantarkan elektron yang cukup banyak untuk dapat menyalakan lampu pada alat uji, dan hanya menimbulkan gelembung gas.
Larutan nonelektrolit terbentuk dari senyawa yang dilarutkan dalam air. Senyawa nonelektrolit dalam air tidak terionisasi, melainkan tetap dalam bentuk molekul, misalnya senyawa nonelektrolit gula dalam pelarut air. Oleh karena tidak ada ion-ion yang bermuatan, maka arus listrik tidak dapat dihantarkan. Hal ini menyebabkan aliran elektron yang menuju lampu menjadi terputus, sehingga lampu tetap tidak menyala.
Bagaimana larutan elektrolit kuat atau elektrolit lemah dapat menimbulkan gejala berupa timbulnya gelembung gas?
Larutan elektrolit mengandung partikel-partikel yang bermuatan (kation dan anion). Berdasarkan percobaan yang telah dilakukan oleh Michael Faraday (1791 – 1867), diketahui bahwa jika arus listrik dialirkan melalui suatu larutan elektrolit akan terjadi proses elektrolisis (elektro = listrik dan lisis = penguraian).
Contoh proses elektrolisis yang terjadi pada larutan HCl akan menghasilkan gas hidrogen dan gas klorin sebagai berikut.
HCl(aq)
|
→
|
H+(aq) + Cl-(aq)
|
2H+(aq) + 2e-
|
→
|
H2(g)
|
2Cl-(aq)
|
→
|
Cl2(g) + 2e-
|
Proses elektrolisis larutan HCl di atas dapat dituliskan sebagai berikut.
2H+(aq) + 2Cl-(aq) → H2(g) + Cl2(g)
Kesimpulan
Berdasarkan daya hantar listriknya, larutan dibedakan menjadi dua yaitu:
1. Larutan Elektrolit
Larutan elektrolit adalah larutan yang dapat menghantarkan arus listrik. ciri-ciri larutan elektrolit adalah menyebabkan nyala lampu dan menimbulkan gelembung gas pada elektroda alat uji daya hantar listrik. Larutan elektrolit dibedakan menjadi dua jenis, yaitu elektrolit kuat dan elektrolit lemah.
Larutan elektrolit kuat menimbulkan gejala nyala lampu terang dan timbul gelembung gas pada elektroda. Contoh larutan elektrolit kuat adalah larutan HCl, H2SO4, air laut, dan air kapur. Sedangkan larutan elektrolit lemah menimbulkan gejala nyala lampu redup dan timbul gelembung gas pada elektroda. Contoh larutan elektrolit lemah adalah larutan amonia, larutan cuka, dan larutan H2S.
2. Larutan Nonelektrolit
Larutan non elektrolit adalah larutan yang tidak dapat menghantarkan arus listrik. Ciri-ciri larutan nonelektrolit adalah tidak menimbulkan nyala lampu dan juga tidak menimbulkan gelembung gas pada elektroda alat uji daya hantar listrik. Contoh larutan nonelektrolit adalah air suling, larutan gula, larutan urea dan larutan alkohol.